10.11.2022
| Dr. Lisa Wild
In diesem Artikel erfahren Sie etwas über den Parameter gelöster Sauerstoff im Allgemeinen und die verschiedenen Messmethoden. Nachdem Sie diesen Text gelesen haben, werden Sie in der Lage sein, den richtigen Sensor für Ihre Anwendung auszuwählen.
Manchmal gibt es einfach zu viele Möglichkeiten, und Sie können sich nicht entscheiden, welches Produkt das richtige für Ihre Anwendung ist. Gelöster Sauerstoff ist ein sehr wichtiger Parameter in vielen Anwendungen wie Abwasserbehandlung, Aquakultur, Industrie sowie Umweltüberwachung und Trinkwasser. Wir unterscheiden hauptsächlich zwischen zwei Messmethoden, der amperometrischen und der optischen Methode. Beide Methoden haben ihre Daseinsberechtigung, allerdings für unterschiedliche Anwendungen und Konzentrationsbereiche. In diesem Artikel werden wir die Grundlagen des gelösten Sauerstoffs erläutern und die Vor- und Nachteile beider Messmethoden in Wasser oder flüssigen Medien diskutieren.
Die elektrochemische Bestimmung von gelöstem Sauerstoff in flüssigen Medien
Die Grundlage für die elektrochemische Bestimmung der Sauerstoffkonzentration sind membranbedeckte elektrochemische Sensoren. [1] Die Hauptbestandteile des Sensors sind die sauerstoffdurchlässige Membran, die Kathode, die Anode, die Elektrolytlösung und eventuell eine Referenzelektrode (Abb. 2). Zwischen der Goldkathode und der Anode, die entweder aus Blei oder Silber besteht, liegt eine Spannung an, die den Sauerstoff zu einer elektrochemischen Reaktion veranlasst. Je höher die Sauerstoffkonzentration ist, desto höher ist auch der resultierende Strom. Die Messgröße ist der Strom im Sensor, der nach einer Kalibrierung in die Konzentration des gelösten Sauerstoffs umgerechnet werden kann. Wenn die Anode aus Silber besteht, liefert das Messgerät die erforderliche Spannung (amperometrischer Sensor). Besteht die Anode aus Blei, handelt es sich um einen selbstpolarisierenden Sensor, d.h. die Spannung wird durch die beiden Elektroden im Sensor selbst erzeugt, ähnlich wie bei einer Batterie (galvanischer Sensor). Das Messgerät wertet nur den Strom aus. Bei der elektrochemischen Bestimmung von Sauerstoff laufen folgende Elektrodenreaktionen ab (Abb. 2).
Der Sauerstoff wird an der Kathode reduziert:
O2 + 2 H2O + 4 e- → 4 OH-
Hier "liefert die Kathode Elektronen" und der durch die Membran diffundierte Sauerstoff reagiert mit den sich bildenden Hydroxid-Ionen.
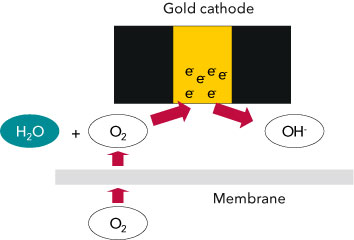
Abbildung 2. Das Prinzip der Elektrodenreaktionen.
Das Elektrodenmetall wird an der Anode oxidiert, wobei folgende Reaktionen ablaufen:
Ag → Ag+ + e-
oder
Pb → Pb2+ + 2 e-
Die Gleichungen der Anodenreaktionen verdeutlichen die Wirkung der Elektrolytlösung. Die Bestandteile der Elektrolytlösung binden die Metallionen, die bei den Anodenreaktionen entstehen. Die Elektrolytlösungen müssen für den jeweiligen Elektrodentyp geeignet sein. Amperometrische Sauerstoffsensoren wie der TriOxmatic® benötigen eine ELY/A-Lösung.
Ag+ + Br- → AgBr ↓
oder
Pb2+ + 2 OH- → 2 Pb(OH)2 ↓
Pb(OH)2 → PbO + H2O
Die dabei entstehenden schwerlöslichen Substanzen bestimmen das elektrochemische Potenzial der Elektrode.
Amperometrische Sensoren können als Dreielektrodenzelle mit einer zusätzlichen Silber/Silberbromid-Elektrode betrieben werden. Sie haben keine Anode im herkömmlichen Sinne mehr. Eine der Silber/Silberbromid-Elektroden übernimmt die Aufgabe der Gegenelektrode (Stromableitung), die andere die Aufgabe einer unabhängigen Referenzelektrode. Diese ist stromlos und weist eine wesentlich bessere Potentialkonstanz auf als eine herkömmliche Elektrode.
Die optische Bestimmung von gelöstem Sauerstoff in Flüssigkeiten
Eine neuere Technologie zur Bestimmung von gelöstem Sauerstoff ist die optische Messung.[2] Ein Sensor zur optischen Messung wird auch als Optode bezeichnet. Mit speziellen Farbstoffen ausgestattete Optoden zeigen optisch messbare Effekte, wenn sie mit den spezifischen Molekülen in Kontakt kommen. Es findet keine Massen- und Energieumwandlung statt, wie zum Beispiel bei den elektrochemischen Sensoren. Es handelt sich lediglich um eine Energieumwandlung, da ein einfallender Lichtstrahl einer bestimmten Wellenlänge in Licht mit einer längeren Wellenlänge und anderen Eigenschaften als das ursprüngliche Licht umgewandelt wird. Diese Art der Reaktion wird als Fluoreszenz bezeichnet (Abb. 3). Dabei werden Farbstoffmoleküle durch Licht angeregt. Bei der Rückkehr in den Grundzustand wird die absorbierte Energie in Form von Licht mit veränderter (größerer) Wellenlänge emittiert. Es gibt Substanzen, die diesen Mechanismus in Abhängigkeit von ihrer Konzentration messbar beeinflussen. Dies sind die so genannten Quencher. Das bedeutet, dass diese Stoffe die Energie des angeregten Zustandes absorbieren, so dass der Farbstoff kein Fluoreszenzlicht mehr aussenden kann und damit "ausgelöscht" wird. Die Intensität des Fluoreszenzlichts wird umso geringer, je höher die Konzentration des Quencher-Moleküls ist.
Dieser Zusammenhang wird im Wesentlichen durch die Stern-Volmer-Gleichung beschrieben:
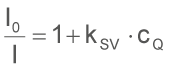
Dabei ist I0 die Lichtintensität ohne den Quencher, I die Intensität mit dem Quencher in einer entsprechenden Konzentration, kSV die Stern-Volmer-Konstante und cQ die Konzentration des Quenchers. Interessant ist in diesem Zusammenhang auch, dass sich nicht nur die Intensität, sondern auch der zeitliche Zerfall des Fluoreszenzlichts nach der Anregung weiterhin entsprechend der Stern-Volmer-Gleichung verhält.
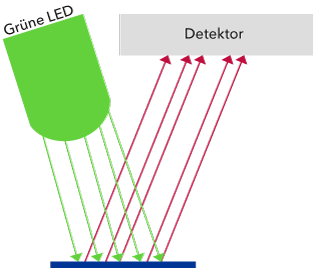
Abbildung 3. Fluoreszenzanregung mit Licht kurzer Wellenlänge (hier grün), Emission eines roten und damit niederenergetischen Fluoreszenzstrahls.
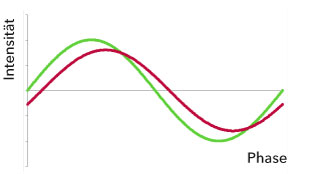
Abbildung 4. Vereinfachte Darstellung des modulierten Stimulus und des emittierten Fluoreszenzstrahls.
Was bedeutet das für die Messung von gelöstem Sauerstoff?
Es gibt Farbstoffe, die durch sichtbares Licht angeregt werden und mit einer hohen Selektivität auf Sauerstoff reagieren. Die Sauerstoffmoleküle dienen als die oben beschriebenen Quencher. Sie löschen oder verändern das vom Farbstoff ausgehende Licht in Abhängigkeit vom Sauerstoffpartialdruck. Mit Hilfe dieses Farbstoffs können geeignete Membranen für die Messung von Sauerstoff in Flüssigkeiten oder Gasen hergestellt werden.
Als Lichtquelle dienen LEDs. Die Anregung der Fluoreszenz erfolgt in modulierter Weise (Abb. 4). Das vom Farbstoff in der Membran emittierte Licht wird erfasst, in ein elektrisches Signal umgewandelt und in ein Sauerstoffsignal umgewandelt.
Grünes Diagramm: periodisch eingestrahltes Licht.
Rotes Diagramm: vom Farbstoff emittiertes Licht in einer verschobenen Phase, die sich aus dem veränderten Abklingverhältnis ergibt.
Vorteile der Sensortypen
Der wesentliche Unterschied zu den amperometrischen Sensoren für gelösten Sauerstoff ist, dass optische Sensoren keinen Sauerstoff verbrauchen. Es finden keine elektrochemischen Reaktionen statt. Hinzu kommt eine weitere Eigenschaft: Der optische Sensor benötigt keine Strömung, um den "verbrauchten" Sauerstoff zu ersetzen. Rührsysteme sind somit überflüssig, was bei Laboranwendungen von Vorteil ist, da diese schnelle Reaktionszeiten erfordern. Elektrochemische Sensoren für die Abwasserbehandlung sind weniger strömungsabhängig und in vielen Fällen ist eine ausreichende Strömung vorhanden. Darüber hinaus entfällt der Elektrolytwechsel und die Reinigung des Elektrodensystems. Die Lebensdauer der FDO® 700 IQ Kappen mit unserer Green-light Technology, die das Ausbleichen des Fluoreszenzfarbstoffs in der Sensormembran verhindert, beträgt mindestens ein Jahr, kann aber zwischen 3 und 5 Jahren liegen.
Elektrochemische Sensoren bilden im Wasser eine 10 µm dicke Schicht aus Wassermolekülen, die nicht aufgerührt werden kann. Daher dient diese Schicht als zusätzliche Diffusionsbarriere. An Luft zeigen diese Sensoren ein Sättigungssignal von etwa 102 %. Der optische Sensor misst an Luft 100 % Sättigung, da diese Barriere hier nicht existiert.
Es kann jedoch sinnvoll sein, die Strömung auch auf einen optischen Sensor anzuwenden. Wie bei allen Systemen mit Grenzflächen findet auch bei der Verwendung des optischen Sensors für gelösten Sauerstoff eine Diffusion des gelösten Sauerstoffs im Wasser in Abhängigkeit von der Konzentration in oder aus der Membran statt. Dieser Prozess ist notwendig, um sich an wechselnde Sauerstoffkonzentrationen anzupassen und läuft umso schneller ab, je besser der Austausch an der Grenzfläche erfolgt. Durch Rühren wird dieser Austausch unterstützt.
Bei optischen Sensoren gibt es keine Polarisationszeit, da sie keine Elektroden haben, die einen Betriebszustand erreichen müssen. Die Polarisationszeit bei elektrochemischen Sensoren ist nicht relevant, wenn galvanische Systeme verwendet werden, die permanent polarisiert sind, auch wenn das Messgerät ausgeschaltet ist.
Optische Sensoren für gelösten Sauerstoff sind Sensoren mit aktiven Komponenten (LEDs, Detektor, Prozessor). Im Gegensatz zu den elektrochemischen Sensoren verbrauchen sie mehr Strom, was bei tragbaren Systemen zu einer deutlich geringeren Betriebszeit führt. Außerdem ist der Messbereich im Vergleich zu den elektrochemischen Sensoren, die bis zu 60 mg/l reichen, deutlich eingeschränkt. Der Grund dafür ist das Quenchen. Vereinfacht gesagt, führt kein Sauerstoff zu einem starken Signal, eine große Menge Sauerstoff zu einem schwachen Signal. Im Allgemeinen überschreitet der Messbereich ca. 200 % Luftsättigung bzw. 20 mg/l nicht.

Abbildung 5. Luftblasen strömen um den FDO® 700 IQ.
Ein Vorteil der FDO® 700 IQ Sensoren ist das sehr stabile Driftverhalten. Sie sind werkskalibriert und müssen im Gegensatz zum TriOxmatic® 700 IQ nicht kalibriert werden.
Durch den eingebauten Speicherchip werden die individuellen Kalibrierdaten vom FDO®-Sensor eingelesen und zur Auswertung verwendet. Somit kann jeder FDO®-Sensor mit jeder Membrankappe kombiniert und ohne Kalibrierung sofort zur Messung verwendet werden.
Im Unterschied zu den amperometrischen Sensoren spielen Kohlendioxid und Schwefelwasserstoff keine Rolle in Bezug auf die Lebensdauer oder Beschädigung der optischen Sensoren. Es ist lediglich zu beachten, dass z.B. Schwefelwasserstoff Querstörungen verursachen kann. Ein Beispiel aus der Praxis wäre der mit zunehmender Tiefe abnehmende Sauerstoffgehalt bei limnologischen Tiefenmessungen, der scheinbar zunimmt, wenn der Sensor in weiches Sediment eingetaucht wird. Der Grund dafür ist jedoch der Schwefelwasserstoff, der bei Fäulnisprozessen in vielen Gewässern entsteht und hier ein Sauerstoffsignal auflöst. Dieses Signal ist reversibel, der Sensor wird nicht geschädigt. Elektrochemische Sensoren sind in Medien vorteilhaft, die organische Flüssigkeiten enthalten, z.B. Abwässer in Industrieanlagen mit Öl oder Lösungsmitteln. Diese Stoffe können die Membran von optischen Sensoren beschädigen.
Optische Sauerstoffsensoren können durch Luftblasen im Medium beeinflusst werden; dieser Einfluss wurde jedoch mit unserer 45°-Technologie für die FDO® Sensoren eliminiert (siehe Abb. 5). Die Membran hat eine horizontale Neigung von 45° und vermeidet die Ansammlung von Luftblasen vor der Membran. Sie sind damit nicht nur kalibrier- und strömungsfrei, sondern auch unempfindlich gegen Luftblasen und benötigen keine zusätzlichen Einbaugeräte.
Wartung und Reinigung der beiden verschiedenen Sensortypen
Die empfindliche Oberfläche eines optischen Sauerstoffsensors ist durch eine lichtdichte Deckschicht geschützt. Diese obere Schicht ist sehr dünn und darf daher nicht zerkratzt oder beschädigt werden, da dies sonst zu Fehlfunktionen führen kann. Die Membran ist bei beiden Sensoren der Teil, der am empfindlichsten auf Verunreinigungen reagiert. Bei leicht anhaftenden Verunreinigungen empfiehlt es sich, die Membran vorsichtig mit einem weichen Mikrotuch zu reinigen. Die Membran des TriOxmatic® ist jedoch robuster und kann auch mit einer Bürste gereinigt werden. Ablagerungen von Kalziumkarbonat oder Eisenoxid können mit 5 bis 10 % (Gewichtsprozent) konzentrierter Essig- oder Zitronensäure aufgelöst werden, und für Fette und Öle kann warmes (<50 °C) Leitungswasser mit Spülmittel verwendet werden. Alkoholische Lösungen sollten zur Reinigung von optischen Membranen nicht verwendet werden, da sie die Membranstruktur beschädigen können. Weitere Hinweise finden Sie in unserer Gebrauchsanweisung.
Wie pflegt man einen optischen Sauerstoffsensor wie den WTW FDO® 700 IQ?
Wie bereits erwähnt, haben die optischen Sauerstoffsensoren ein sehr stabiles Driftverhalten, und die Veränderungen durch das eingestrahlte Licht sind im Allgemeinen viel kleiner als 5 % des Ausgangswertes im Laufe eines Jahres. Wenn diese Toleranz akzeptiert werden kann, muss der Sensor nicht kalibriert werden.
Die Kappen des FDO® 700 IQ müssen alle 3 bis 5 Jahre ausgetauscht werden. Wir versehen die Wechselkappen, die der Anwender einfach auf den Sensor aufsteckt, mit Farbstoff. Diese Wechselkappen enthalten einen Chip mit den im Produktionsprozess ermittelten Spezifikationen der jeweiligen Membran ("Werkskalibrierung"). Diese Daten werden automatisch auf den Sensor übertragen und für die korrekte Berechnung der Sauerstoffkonzentration verwendet. Selbstverständlich ist auch eine Kalibrierung durch den Anwender möglich. Sie wird analog zu den elektrochemischen Sensoren in wasserdampfgesättigter Luft im Kalibriergefäß durchgeführt. Wie bereits oben erwähnt, liegt die resultierende Sättigungsanzeige bei 100 %.
Wie pflegt man einen elektrochemischen Sauerstoffsensor wie den WTW TriOxmatic® 700 IQ?
Die elektrochemischen Sensoren erfordern je nach Anwendung einen Austausch der Membran und des Elektrolyten, können aber bis zu 5 Jahre ohne Wechsel der Membrankappe betrieben werden. Außerdem sollte die Goldkathode des elektrochemischen Sensors einer Sichtprüfung unterzogen werden. Ist sie nicht mehr goldfarben, sondern mit Blei oder Silber überzogen, zeigt der Sensor hohe Werte an und ist in der Regel nicht mehr stromfrei. Abhilfe schafft das Regenerieren des Gelöstsauerstoffsensors gemäß der Bedienungsanleitung. Die Goldkathode sollte nur mit einem speziellen, angefeuchteten Polierstreifen mit kreisenden Bewegungen und wenig Druck poliert werden. Nur dieser Streifen darf auf jeden Fall verwendet werden, da eine zerkratzte und unpolierte Elektrodenoberfläche den Sensor beschädigt und die Messsicherheit negativ beeinflusst.
Der optische Sensor (FDO® 700 IQ) muss nicht kalibriert werden, da er werkseitig kalibriert ist und während der gesamten Lebensdauer des Verschlusses (mindestens ein Jahr) stabil bleibt. Eine Kalibrierung kann jedoch durchgeführt werden, wenn dies für die Einhaltung von Vorschriften oder die Qualitätssicherung erforderlich ist. Der elektrochemische Sensor (TriOxmatic® 700 IQ) sollte zweimal pro Jahr oder je nach Anwendung kalibriert werden. Bei beiden Sensoren erfolgt die Kalibrierung in wasserdampfgesättigter Luft. Dazu sollte der Sensor ca. 2 cm über einer Wasseroberfläche positioniert werden, z.B. in einem schmalen Eimer oder einem ähnlichen Behälter mit Wasser. Bei Lufttemperaturen unter 5 °C empfehlen wir, nicht in Luft, sondern in luftgesättigtem Wasser, das eine höhere Temperatur hat, zu kalibrieren. Luftgesättigtes Wasser erhält man, indem man aus zwei Gefäßen mehrmals Wasser ein- und ausgießt, so dass es sprudelt.
Zusammenfassend lässt sich sagen, dass die optischen Sensoren hauptsächlich Vorteile gegenüber den amperometrischen Sensoren bieten. Da die optischen Sensoren FDO® strömungsfrei und unempfindlich gegenüber Luftblasen sind und keine Kalibrierung benötigen, sind optische Sensoren oft der optimale Sensor zur Messung von gelöstem Sauerstoff in Abwasser, Oberflächenwasser, Trinkwasser und Aquakulturen in einem Messbereich von bis zu 20 mg/l. Aber auch unser amperometrischer Sensor TriOxmatic® 700 IQ kann in verschiedenen Anwendungen von Vorteil sein, da er chemisch und physikalisch robuster ist, weniger Energie benötigt und einen größeren Messbereich mit gelösten Sauerstoffkonzentrationen von bis zu 60 mg/l oder 600 % hat.
Wenn Sie weitere Informationen benötigen, finden Sie unten Anwendungsberichte über optische oder amperometrische Sensoren sowie über die Validierung von Sauerstoffsensoren hier als Download.